Biologie du système neuromusculaire
Présentation

Équipe Relaix de l'Institut Mondor de Recherche Biomédicale
 Nous étudions les muscles squelettiques du corps qui permettent à un individu de tenir une posture, de se déplacer, d'exécuter des mouvements, de se réchauffer et de respirer. Ces muscles sont sous contrôle volontaire du système nerveux central et c'est pourquoi on parle du système neuromusculaire. Lorsque le muscle ne se développe pas harmonieusement ou dysfonctionne, on parle de myopathies ou de maladies neuromusculaires. Ces maladies, parfois mortelles et très souvent invalidantes, touchent spontanément des enfants, des adultes, des animaux domestiques et restent aujourd’hui majoritairement sans traitement.
Nous étudions les muscles squelettiques du corps qui permettent à un individu de tenir une posture, de se déplacer, d'exécuter des mouvements, de se réchauffer et de respirer. Ces muscles sont sous contrôle volontaire du système nerveux central et c'est pourquoi on parle du système neuromusculaire. Lorsque le muscle ne se développe pas harmonieusement ou dysfonctionne, on parle de myopathies ou de maladies neuromusculaires. Ces maladies, parfois mortelles et très souvent invalidantes, touchent spontanément des enfants, des adultes, des animaux domestiques et restent aujourd’hui majoritairement sans traitement.
Nos recherches visent à offrir aux médecins et aux vétérinaires des outils médicaux moléculaires ou cellulaires leur permettant d'éviter l'apparition de ces maladies et quand malheureusement elles suviennent, de les diagnostiquer avec précision pour les traiter avec plus d'efficacité et de durabilité. Nous travaillons sur les maladies neuromusculaires animales et humaines, convaincus que cette médecine comparée bénéficie à nos animaux domestiques et aux patients en améliorant en parallèle le bien-être des animaux et le mieux vivre des patients et des familles.

L'EnvA

Hôpital Mondor de Créteil
Notre équipe de 110 médecins, vétérinaires, universitaires, chercheurs, doctorants, stagiaires, personnels techniques et administratifs, est structurée en sept groupes localisés sur le campus de l'EnvA (groupes 3 et 4), et le campus de l'hôpital Mondor de Créteil (groupes 1, 2, 5, 6 et 7)
EN SAVOIR +
Direction et contacts :
Directeur : Frédéric Relaix
Responsables des groupes 3 et 4 sur le campus de l'EnvA :
Laurent Tiret et Stéphane Blot

Responsables de groupes, de gauche à droite : Hélène Rouard (gp 5, Mondor), Stéphane Blot (gp 4, EnvA),
Frédéric Relaix (gp 1, Mondor), Laurent Tiret (gp 3, EnvA et Mondor) et Jérôme Authier (gp 2, Mondor).
Crédit : Christophe Hargoues
Organigramme :
Télécharger le fichier
Thèmes de Recherche
Notre activité de recherche se décline en trois thèmes majeurs :

Caractérisation phénotypique et génétique des maladies neuromusculaires chez l'homme et les modèles animaux, en particulier les chiens et chats de propriétaires qui viennent en consultation, spontanément atteints par ces maladies au cours de leur vie.
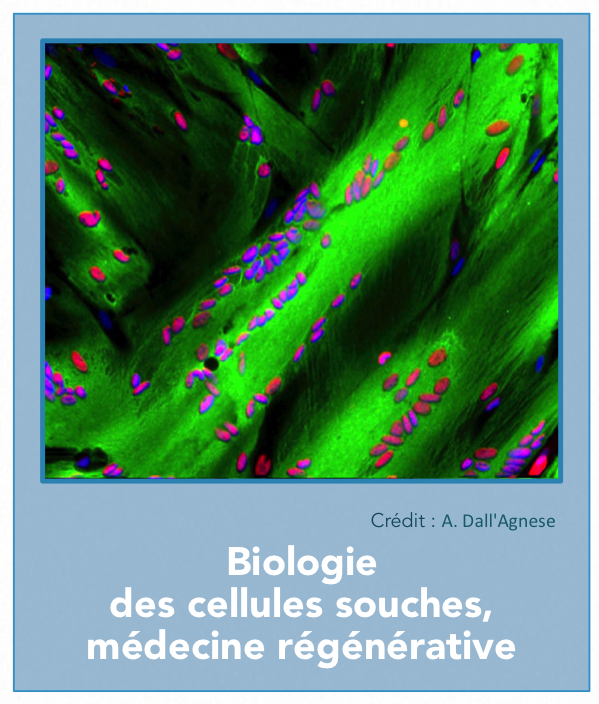
Élucidation pour la cellule souche musculaire des mécanismes moléculaires intrinsèques ou dépendants de sa niche cellulaire qui contrôlent sa quiescence ou sa spécification, son développement, son vieillissement et son exposition aux modulateurs internes ou environnementaux.

Identification ou validation de l’efficacité et l’innocuité d'outils thérapeutiques innovants pour les maladies neuromusculaires en intégrant dans une même équipe les phases d'essais précliniques chez l’animal et cliniques chez l’homme.
Publications
Sélection d'articles récents et représentatifs des activités de l'équipe.
Une liste complète des articles publiés depuis 2012 est disponible en fin de section.
- Prola, A., Blondelle, J., Vandestienne, A., Piquereau, J., Denis, R.G.P., Guyot, S., Chauvin, H., Mourier, A., Maurer, M., Henry, C., Khadhraoui, N., Gallerne, C., Molinié, T., Courtin, G., Guillaud, L., Gressette, M., Solgadi, A., Dumont, F., Castel, J., Ternacle, J., Demarquoy, J., Malgoyre, A., Koulmann, N., Derumeaux, G., Giraud, M.-F., Joubert, F., Veksler, V., Luquet, S., Relaix, F., Tiret, L. & Pilot-Storck, F. (2021). Cardiolipin content controls mitochondrial coupling and energetic efficiency in muscle. Science Advances 7, eabd6322.
Lien : https://advances.sciencemag.org/content/7/1/eabd6322
- Barthélémy, I., Calmels, N., Weiss, R.B., Tiret, L., Vulin, A., Wein, N., Peccate, C., Drougard, C., Beroud, C., Deburgrave, N., Thibaud, J.-L., Escriou, C., Punzón, I., Garcia, L., Kaplan, J.-C., Flanigan, K.M., Leturcq, F. & Blot, S. (2020). X-linked muscular dystrophy in a Labrador Retriever strain: phenotypic and molecular characterisation. Skeletal Muscle 10, 23.
Lien : https://doi.org/10.1186/s13395-020-00239-0
- Prokic, I., Cowling, B.S., Kutchukian, C., Kretz, C., Tasfaout, H., Gache, V., Hergueux, J., Wendling, O., Ferry, A., Toussaint, A., Gavriilidis, C., Nattarayan, V., Koch, C., Lainé, J., Combe, R., Tiret, L., Jacquemond, V., Pilot-Storck, F. & Laporte, J. (2020). Differential physiological role of BIN1 isoforms in skeletal muscle development, function and regeneration. Disease Models & Mechanisms.
Lien : https://dmm.biologists.org/content/early/2020/09/25/dmm.044354
- Temmam, S., Barbarino, A., Maso, D., Behillil, S., Enouf, V., Huon, C., Jaraud, A., Chevallier, L., Backovic, M., Pérot, P., Verwaerde, P., Tiret, L., van der Werf, S. & Eloit, M. (2020). Absence of SARS-CoV-2 infection in cats and dogs in close contact with a cluster of COVID-19 patients in a veterinary campus. One Health 10, 100164.
Lien : http://www.sciencedirect.com/science/article/pii/S2352771420302652
- Der Vartanian A, Quetin M, Michineau S, Aurade F, Hayashi S, Dubois C, Ronancourt D, Drayton-Libotte B, Szegedi A, Buckingham M, Conway SJ, Gervais M, Relaix F. 2019 PAX3 confers functional heterogeneity in skeletal muscle stem cell responses to environmental stress. Cell Stem Cell. pii: S1934-5909(19)30118-3.
- Barthélémy I, Hitte C, Tiret L. 2019 The dog model in the spotlight: legacy of a trustful cooperation.Journal of Neuromuscular Diseases. Pre-press 10.3233/JND-190394.
- Briand A, Cochet‐Faivre N, Reyes‐Gomez E, Jaraud‐Darnault A, Tiret L, Chevallier L. 2019 NIPAL4 deletion identified in an American Bully with autosomal recessive congenital ichthyosis and response to topical therapy. Veterinary Medicine and Science 5, 112–117.
- Fabrès V, Dossin O, Reif C, Campos M, Freiche V, Maurey C, Pilot-Storck F, Desquilbet L, Benchekroun G. 2019 Development and validation of a novel clinical scoring system for short-term prediction of death in dogs with acute pancreatitis. J Vet Intern Med. 33(2), 499-507.
- Alonso-Martin S, Auradé F, Mademtzoglou D, Rochat A, Zammit PS, Relaix F. 2018 SOXF factors regulate murine satellite cell self-renewal and function through inhibition of β-catenin activity. Elife. 7, pii e26039.
- Aoun Sebaiti M, Kauv P, Charles-Nelson A, Van Der Gucht A, Blanc-Durand P, Itti E, Gherardi RK, Bachoud-Levi AC, Authier FJ. 2018 Cognitive dysfunction associated with aluminum hydroxide-induced macrophagic myofasciitis: A reappraisal of neuropsychological profile. J Inorg Biochem. 181, 132-138.
- Baghdadi M, Castel D, Machado L, Fukada SI, Birk DE, Relaix F, Tajbakhsh S, Mourikis P. 2018 Notch/CollagenV/CalcR reciprocal signalling retains muscle stem cells in their niche.Nature. 557(7707), 714-718.
- Filareto A, Maguire-Nguyen K, Gan Q, Aldanondo G, Machado L, Chamberlain JS, Rando TA. 2018 Monitoring disease activity noninvasively in the mdx model of Duchenne muscular dystrophy.Proc Natl Acad Sci USA. 115(30), 7741-7746.
- Mademtzoglou D, Asakura Y, Borok MJ, Alonso-Martin S, Mourikis P, Kodaka Y, Mohan A, Asakura A, Relaix F. 2018 Cellular localization of the cell cycle inhibitor Cdkn1c controls growth arrest of adult skeletal muscle stem cells. Elife 7, pii e33337.
- Morgan JE, Prola A, Mariot V, Pini V, Meng J, Hourde C, Dumonceaux J, Conti F, Relaix F, Authier FJ, Tiret L, Muntoni F, Bencze M. 2018 Necroptosis mediates myofibre death in dystrophin-deficient mice. Nat Commun. 9(1), 3655
- Le Guiner C, Servais L, Montus M, Larcher T, Fraysse B, Moullec S, Allais M, François V, Dutilleul M, Malerba A, Koo T, Thibaut J-L, Matot B, Devaux M, Le Duff J, Deschamps J-Y, Barthelemy I, Blot S, Testault I, Wahbi K, Ederhy S, Martin S, Veron P, Georger C, Athanasopoulos T, Masurier C, Mingozzi F, Carlier P, Gjata B, Hogrel J-Y, Adjali O, Mavilio F, Voit T, Moullier P, Dickson G. 2017 Long-term microdystrophin gene therapy is effective in a canine model of Duchenne muscular dystrophy. Nat Commun 8. 16105.
Télécharger une liste complète des articles publiés par les membres de l'équipe ICI
Partenaires
Partenaires institutionnels
Joint Research Team in “Biology of the neuromuscular system
(UPEC-INSERM-EnvA-EFS; Head: F. Relaix)
This large translational Team is focusing on neuromuscular disorders, from basic to clinical research, including pathophysiological studies, animal models modeling, tissue engineering and therapeutic approaches. Five main axis are developed:
- Molecular mechanisms regulating muscle stem cell development and functions, and interactions with the local and systemic environment
- Tissue engineering of musculoskeletal disorders using muscle and mesenchymal stem cells.
- Pathophysiological and clinical research of neuromuscular disorders, including myotonic dystrophies, macrophagic myofascitis and Duchenne muscular dystrophy.
- The veterinary geneticians are also investigating the genetic bases of canine and feline neuro-muscular disorders, with potential applications for both animal and human healths.
- Canine and feline models of human myopathies are also deeply investigated, in particular for the preclinical evaluation of unique therapeutic strategies, such as exon skipping approaches.









